抗乙肝新药阿德福韦研究情况
乙型肝炎仍然是威胁健康的全球性问题。每年约有120万人死于乙型肝炎及其相关疾病,慢性乙肝携带者占全球人口的5%。目前有两种基本方式治疗慢性乙型肝炎,一种是免疫激活治疗如干扰素,另一种是抑制病毒复制如已经上市的贺普丁。阿德福韦双异戊酰氧甲酯(Adefovir dipivoxil, 简称ADV)是一种新的抗乙肝病毒(HBV)的药物。去年9月经FDA批准在美国上市, 是继拉米夫定后的另一个口服的抗HBV药物。ADV属单磷酸腺苷磷酸核苷酸类似物,其化学名是:9-[-2<双·[三甲基乙酰氧)甲氧基]氧磷基]甲氧基]乙基]腺嘌呤,分子式为C20H32N5O8P, 分子量为501.48,化学结构见图1 。
抗病毒谱
临床前抗病毒研究表明,ADV在体外和体内对乙肝病毒(HBV),鸭乙肝病毒(DHBV),美洲旱獭肝炎病毒(WHV),以及对拉米夫定及其它抗HBV药物出现耐受变异株的乙肝病毒均有很强的抗病毒活性,对逆转录病毒,人类免疫缺陷病毒(HIV)以及疱疹病毒也有很强的抗病毒活性。
药理和毒理
ADV100mg/kg对小鼠的总体行为没有影响(Irwin试验);ADV30-100mg/kg在大鼠中出现尿量和电介质排泄减少;任何剂量都不影响大鼠的胃肠蠕动;剂量12mg/kg对麻醉状态狗的心血管和呼吸功能无影响。 抑制DNA g多聚酶(与DNA合成有关)Ki在ddCTP, FIAUTP, AZTTP和ADV分别为0.034,0.031,18.3和299mM。与ddC, FIAU或AZT比较,ADV对线粒体毒性较低。(1)
ADV 体外能有效抑制病毒DNA多聚酶,从而抑制HBV的复制。口服阿德福韦后,首要的毒性靶器官依次为肾、胃肠道,肝脏和淋巴增生组织(包括骨髓)。大鼠和猴服用ADV后,肾毒性是主要的剂量限制相关毒性。剂量10mg/kg,在小鼠中没有发现与ADV相关致癌性。剂量5mg/kg,在大鼠中未发与药物相关致癌性。剂量2.5mg/kg ,在妊娠大鼠研究中对胚胎发育无明显影响。阿德福韦对胚胎发育以及产前和产后的影响,仅表现在大剂量造成妊娠大鼠中毒时(20mg/kg/天)才观察到,此时的剂量相当于人类剂量的38倍。ADV在遗传毒性方面与其他核苷类似物相似。
动物药代动力学
已在小鼠,大鼠,猴中观察阿德福韦的吸收、分布、代谢和排泄。口服阿德福韦后,在0.5-1.5小时达到最大血药浓度,随后呈两相下降。观察到的终末半衰期为6小时(范围4-6小时)。大鼠的生物利用度最大,猴最小。没有检测出阿德福韦的循环代谢物,这与阿德福韦不以肝肠代谢为主相一致。在动物模型中,ADV可分布于大部分组织。其中肠、肝、肾浓度最高。 在排除前,ADV不会被代谢。ADV通过肾小球滤过和肾小管分泌相结合的形式由肾脏以原形排泄。
药效学
阿德福韦在体外HepG2和HB611肝癌细胞株中有抗人乙肝病毒活性, IC50为0.2-1.2mM,CC50为100-150mM。在原代鸭肝细胞株中,IC50为0.01-0.4mM,CC50>100mM。美洲旱獭的IC50<1mM, CC50未作检测。
抗病毒作用机制
ADV经细胞内激酶磷酸化形成有活性的二磷酸盐。该活性代谢产物可竞争抑制HBV DNA多聚酶,从而抑制病毒复制。整合阿德福韦进入病毒DNA链,链合成随之终止。其所需要的药物浓度仅为0.1mM,远低于抑制人类DNA多聚酶a(1.18mM)、g(0.97mM)的浓度。核苷类似物如拉米夫定或泛昔洛韦,在转化成有活性形式的三磷酸盐之前,需依赖于细胞型或细胞特异的核酸激酶,在细胞内先转化成单磷酸盐的形式。而ADV本身含有单磷酸盐基团,较之更易转化,所以与其它核苷类似物比较,阿德福韦可能对更多的细胞种类有抗病毒的活性。阿德福韦二磷酸盐在细胞内的半衰期大约为12-36h,这也支持临床上常规每日给药一次。
临床药代动力学
在健康受试者和慢性乙型肝炎病人中进行ADV(10mg)的药代动力学研究,两组人群药代动力学特征相似。ADV口服吸收迅速,在空腹状态下,最大峰浓度(Cmax)的平均值范围:17.5-21.3ng/ml,达峰时间(Tmax)(中位数):0.76-1.75小时。曲线下面积(AUC)平均值范围:178-210ng·hr/ml。与食物同服,达峰时间可延迟2小时。但并不影响达峰浓度(Cmax)和曲线下面积(AUC)。阿德福韦10mg的口服生物利用度估计为59%。在慢乙肝病人中,ADV稳态和单剂量的药代动力学特征没有明显差异。在动物模型中,ADV可分布于大部分组织。其中肠、肝、肾浓度最高。静脉给药,剂量范围:1.0-3.0mg/kg,阿德福韦稳态的分布容积为418-76ml/kg。体外研究显示,阿德福韦对血浆和血清蛋白的蛋白结合率很低。阿德福韦浓度范围从0.25mg/ml到25mg/ml,蛋白结合率平均值£4%。阿德福韦口服后,首先通过细胞内激酶磷酸化,形成二磷酸盐。在消除前,阿德福韦不会被代谢。在体外,阿德福韦或其活性形式都不会影响人体细胞色素P450,提示阿德福韦10mg不会对那些经肝脏转化的药物以及在肾脏消除的药物不存在有临床意义的相互作用。 ADV通过肾小球滤过和肾小管分泌相结合的形式从肾脏以原形排泄。ADV终末半衰期为6-7小时。ADV10mg未在儿童中进行研究,但在38例4个月至18岁的HIV感染者中发现ADV(1-3mg/kg)的表观清除率高于成年人。中重度肝功能不全(child-pugh-turcotte: B,C级)的病人无需调整阿德福韦的剂量。 对肾功能不全(肌酐清除率<50ml/分)的病人需进行剂量调整。在已有的资料表明,ADV的药代动力学在不同人种/种族、性别、年龄或体重之间没有明显差异。
临床试验
最初的临床研究选择 HBeAg(+) 的慢乙肝病人共20例,其中13例合并HIV感染,随机,双盲分配进入ADV125mg(口服每日一次)治疗组和安慰剂组治疗28天,ADV治疗组HBV DNA平均下降1.8 log10pg/ml, 而安慰剂组平均上升0.01 log10pg/ml。 治疗组有1例病人在治疗期间eAg转阴,停药后12周检测eAb阳性。研究表明ADV能有效降低血清HBV DNA,病人在研究过程中表现出良好的耐受性。(2)
选择515例 HBeAg (+)慢乙肝病人,分别随机,双盲分配进入ADV10mg, 30mg和安慰剂组治疗48周。ADV10mg与30mg组与安慰剂组比较,在肝组织学表现、HBV DNA、ALT、eAg阴转等各项目均有明显的改善,在统计学上均有显著性差异(p<0.001)。 eAb阳性者10mg组为12%,30mg组为14%,分别与安慰剂组6%比较(p=0.049和p=0.011)。ADV10mg组与安慰剂组的安全性相似,48周治疗结束时,10mg组与安慰剂组病人血清肌酐平均值较基线没有升高,30mg组较基线升高0.2mg/dl(18mmol/L)。10mg组和安慰剂组没有病人出现血清肌酐较基线水平升高3 0.5mg/dl(44mmol/L),30mg组有8%病人出现(p<0.001)。所有出现肾损表现的病人在调整剂量或中止治疗后,肾功能都恢复正常。ALT升高>正常上限值10倍的病人,在10mg组为10%,30mg组为8%,安慰剂组为19%,均无伴随总胆红素,白蛋白或凝血酶原时间的变化。治疗结束后,病人重新分组,分别进入ADV10mg治疗组和安慰剂组,72周评估时发现,继续服用ADV10mg治疗的病人中44%出现eAg转阴,23%出现eAb阳性。其安全性评估结果与前48周结果相类似。(3)
ADV治疗拉米夫定耐药的慢乙肝病人有较好疗效,把拉米夫定耐药的病人分成三组,分别给予拉米夫定,拉米夫定+ADV,ADV治疗,在两组ADV治疗的病人均出现明显的DNA下降(p<0.001),ALT复常率明显高于单用拉米夫定组(p<0.005)。在48周时,拉米夫定组未出现eAg和eAb的转换,而合用组和单用ADV组eAg阴转率分别为17%和16%,eAb阳性者为6%和11%。(4)
对拉米夫定耐药,YMDD出现变异的失代偿性肝硬化的40例慢乙肝病人,给予拉米夫定+ADV研究,其中1例因肝衰竭,2例因肌酐清除率下降而停药,其余病人均完成52周的治疗,90%的病人DNA≤105拷贝/ml或比基线时DNA下降≥2log10拷贝/ml,53%的病人ALT复常,30%的病人eAg阴转,4%的病人出现eAb阳转。(5)
慢乙肝肝移植的病人,在移植前后服用ADV,可以明显降低HBV DNA,改善肝功能及凝血酶原时间,生存率提高,副反应发生率较低。在服用ADV的病人中,一部分出现肌酐(Cr)的升高,大多伴有其它的多重危险因素,例如使用免疫抑制剂和/或其它肾毒性药物,导致许多病人在ADV治疗前就有潜在的肾功能损害表现(肌酐清除率<80ml/min)。其中大部分在调整剂量后仍能安全服用ADV,约有2%的病人因严重肾功能损害而停药。国外报道一例病人,由于本人是麻醉医师,在工作中被针头刺到,而感染慢乙肝,曾用干扰素治疗,因不能耐受而中止。用拉米夫定治疗产生YVDD变异。由于出现肝功能衰竭,于1996年进行肝移植。由于慢乙肝复发,病人的ALT和DNA水平明显升高,临床情况再度恶化,出现轻度腹水。2000年5月开始ADV10mg治疗,3个月后HBV DNA明显下降,临床表现改善,ALT和凝血酶原时间逐渐复常。(6)
由于ADV对肾功能有潜在危害,目前报道用ADV治疗慢乙肝的病人在治疗前均无明显肾功能损害。现在有一例肝移植伴终末期肾衰的病人,服用ADV治疗的报告。病人33岁,因慢乙肝导致肝硬化于1993年进行肝移植,后乙肝复发。1995年病人开始服用拉米夫定每天100mg, 直到1999年11月,YMDD(M550V和L526M)变异。2000年停用拉米夫定,给予ADV治疗,由于发现病人的肾功能有严重损害(这与病人接受肝移植后一直使用免疫抑制剂有关),而ADV有潜在的肾损作用,所以用药的第二天就停药了。病人随后的临床症状逐渐恶化,凝血酶原时间延长,黄疸出现,肝活检为肝硬化和纤维性瘀胆性表现,病人出现危险的持续性细菌性腹膜炎,医师对ADV的肾损危险和治疗效益重新评估,决定给病人服用ADV,剂量调整为每次透析后给予10mg口服,病人DNA水平明显降低,最后用PCR定量方法测不出(Amplicor HBV),Child-Pugh评分在一个月内从12降低5,临床症状和实验室指标明显改善,病人重返工作岗位,全天工作,不需要等候肝移植。肾功能也有改善,肌酐清除率从原来的8ml/min增加到16ml/min, 每周两次透析仍在进行。18个月治疗后,HBeAg转阴,HBeAb未阳转,治疗12个月后肝活检发现纤维性瘀胆表现消失,仅有轻度炎症表现。(7)
ADV治疗达136周,尚未出现耐药性。研究表明在ADV治疗48周后继续服药,可以持续抑制DNA, eAg阴转率增加,肝功能各项指标持续改善。 由于ADV是一个临床应用时间较短的新药,且病人的标本数量还比较少,将来是否会出现病毒变异,仍需临床和实验室的严密观察。
已有的安全性资料表明,ADV10mg组与安慰剂组在不良事件及实验室检测值异常的种类、发生频率、严重程度相似,其中不包括ALT升高,后者发生在安慰剂组的频率较高。所有不良事件或实验室检查异常的发生率并未由于治疗时间延长(48周延至96周)而增加。不良反应中常见的是:头痛,咽炎,无力,腹痛及流感样症状,发生率>10%。 ADV10mg组发生的严重不良反应和因此停药的发生率与安慰剂组相似。
适应症、剂量和用法
目前ADV已经美国药品与食品监督管理局(FDA)批准,适用于成年人伴有病毒复制和/或ALT、AST持续升高,或肝组织学为活动性病变的慢乙肝治疗。HBeAg阳性或阴性、肝功能没有失代偿的慢乙肝病人均适用。拉米夫定耐药的慢乙肝病人可以应用。剂量为10mg,每日口服一次,不受食物影响。疗程暂时未定。
注意事项
值得注意的是,有25%的慢乙肝病人在停药后ALT升高超过正常上限值的10倍以上,大多在停药后12周内出现,病人在治疗期间无HBeAg阴转。病人治疗前肝功能表现为代偿性, ALT升高通常为自限性或通过其它对症治疗可以缓解,不会导致肝功能失代偿。如果病人已有失代偿表现,则ALT升高可能导致临床恶化,甚至死亡。所以临床医师对停药后病人应密切观察,定期检测肝功能各项指标,及时发现异常,采取措施,缓解症状。其次,在以前ADV60mg和120mg治疗HIV以及30mg治疗慢乙肝的临床研究中,发现ADV对肾脏有潜在的毒性。ADV10mg治疗慢乙肝也可能出现类似表现。主要是血清肌酐(Cr)升高,血磷(P)降低。用药期间应严密监测病人的肾功能指标,如Cr,尿素氮(BUN),血磷及其它电介质等,特别是病人同时服用对肾脏有损害的的药物如免疫抑制剂等。对肾功能损害的病人用药剂量调整如下:
内生肌酐清除率血液透析≥5020-4910-19病人10mg10mg10mg10mg每24小时每48小时每72小时每7天于血液透析后
治疗前检测HIV抗体,因为ADV10mg不足以抑制HIV RNA,可能在治疗慢乙肝的同时,出现HIV耐药性。另外还有因高乳酸血症和严重的肝肿大伴脂肪变性导致死亡的报告,大部分发生在女性,肥胖和长期应用核苷类药物是高危因素。 ADV治疗的病人慎用影响肾功能的药物。ADV治疗对长期预后(如原发性肝癌或失代偿性肝硬化)的影响尚未明确 。ADV对妊娠病人的影响还在评估中,目前建议对这类病人不要应用。产后病人若服用ADV,建议放弃母乳喂养。老年病人应谨慎使用,特别是因肾功能降低或合并心血管疾病而用药的,更应密切观察。
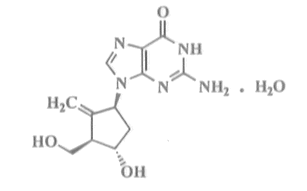
图1 阿德福韦的化学结构
参考文献
1. Cherrington JM, Allen SJ, McKee BH, et al. Kinetic analysis of the interaction between the diphosphate of (S)-1-(3-hydroxy-2-phosphonylmethoxypropyl) cytosine, ddCTP, AZTTP, FIAUTP with human DNA polymerases beta and gamma. Biochem Pharmacol 1994; 48: 1986-1988.
2. Gilson RJ, Chopra KB, Newell AM, et al. A placebo-controlled phase I/II study of adefovir dipivoxil in patients with chronic hepatitis B virus infection. J Viral Hepat 1999;6: 387-395.
3. Patrick M, Ting-Tsung C, Seng GL, et al. Adefovir dipivoxil for the treatment of hepatitis B e antigen-positive chronic hepatitis B. N Engl J Med 2003; 348;9: 808-816.
4. Marion P, H. W. Hann, P. Martin, et al. Adefovir dipivoxil(ADV) alone and in combination with lamivudine(LAM) suppress YMDD mutant hepatitis B virus replication: 48 week preliminary analysis. Hepatology 2002;36: 374A.
5. David M, Hie-Won LH, Maria B, et al. Significant clinical improvement following the addition of adefovir dipivoxil to lamivudine in decompensated patients with YMDD variant HBV and a reduced response to lamivudine. Hepatology 2002;36: 625A.
6. Erica V, Valentina B, Antonella G, et al. Predominance of Pre-S1 mutated hepatitis B virus in a patient following treatment with adefovir dipivoxil. Liver Transplantation2003;9: 188-190.
7. Hans LT, C. Thomas B, Jorg SB, et al. Successful treatment of fibrosing cholestatic hepatitis using adefovir dipivoxil in a patient with cirrhosis and renal insufficiency. Liver Transplantation2003;9: 191-196.
感谢:葛兰素 史克公司提供资料。
下一篇:治疗性乙肝疫苗