ESPGHAN:儿童慢性乙肝诊治指南
儿童慢乙肝诊治指南(全文)
作者:伊文 来源:肝脏病学杂志中文版 日期:2014-03-18
在世界范围内大约有3.6 亿(占世界总人口的6%)乙型肝炎病毒(hepatitis B virus,HBV)慢性感染者。尽管随着乙肝疫苗免疫接种计划在许多国家得到普及和实施以及对献血员的筛查,HBV 的感染率已经大幅度下降,但每年仍有大量的儿童感染HBV,且常常发展为慢性感染,需要得到相应的随访观察。虽然慢性乙型肝炎在儿童或青少年时期是一个相对良性的过程,但在成人之前仍然分别有3%~5% 和0.01%~0.03% 的慢性携带者发展为肝硬化和肝细胞癌。
成人患者已经有了安全有效的抗病毒治疗,但几乎没有药物注明可应用于儿童,也没有告诉人们哪些患儿需要治疗,或什么时候进行治疗,从而优化治疗应答,减少耐药的风险。尽管国际上几个主要的专业学会发布了多部成人CHB 诊疗指南,但儿童乙肝的诊疗仍需进一步完善。
由欧洲儿科胃肠病、肝病、营养学会(European society of Pediatric Gastroenterology, Hepatology and Nutrition,ESPGHAN)挑选专家组共同编写《儿童慢性乙型肝炎诊治指南》。该指南提出推荐的证据主要基于2012 年6 月份之前公开发表的学术论文。如果不能获得证据,则依据专家个人经验。指南作者对证据进行评估并进行分级,分级证据见表1。
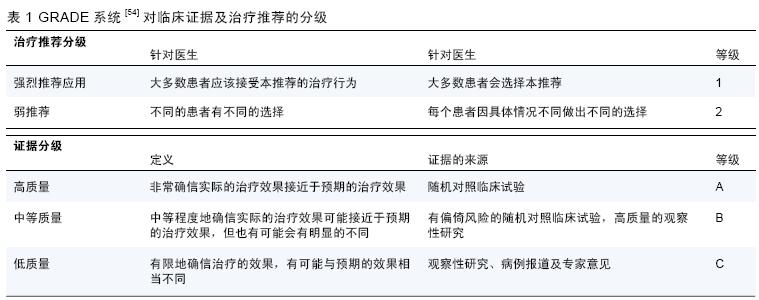
治疗终点及应答的定义
儿童和成人抗HBV 治疗的目标都是通过减少肝病进展、肝硬化及HCC 的风险来改善长期生存率和生活质量。对所有患者来说,理想的治疗终点是持续HBsAg 清除,因为这样可中止疾病进展,减少HCC 的风险,尽管这种理想的情况只发生在极少数接受治疗的患者(A1)。
如果没有获得HBsAg 血清学清除,对于HBeAg 阳性患者,停止治疗后持续病毒抑制(用敏感的实时PCR试剂测不出HBV DNA)和与此相关的持久的HBeAg 血清学转换,也是一个好的终点,与预后的改善包括降低HCC 的风险相关(A1)。
如果不能达到停药后的病毒抑制,那么通过长期抗病毒治疗(维持病毒学应答)使HBV DNA 测不出,是次级理想终点。病毒血症的下降引起肝脏炎症缓解, ALT 水平随之复常,疾病进展的风险降低。
治疗应答可在生化学、血清学、病毒学及组织学水平上评估。在很少的几项儿童药物临床试验中,有几个治疗终点被用于评估治疗的应答。有关应答的定义,需要达成共识,方能对不同的临床试验进行比较。目前美国肝病研究学会(American Association for the Study of Liver Disease,AASLD)或欧洲肝病研究学会(European Association for the Study of the Liver,EASL)对治疗应答的定义可应用于儿童药物临床试验:
生化学应答:ALT 复常,反映了组织学活动指数降低。但ALT 水平是一个较难评价的指标,因为ALT 水平可在较长时间内大幅度波动,并且在出现HBeAg 血清学转换后仍持续升高达6~12 个月。因此,在治疗结束后的第一年里每3 个月应检测一次ALT(C1),治疗结束后第二年里每6 个月检测一次ALT(C2)。
HBeAg 的血清学应答定义为HBeAg 消失及血清学转换为抗HBe(只适用于HBeAg 阳性患者);HBsAg 血清学应答定义为HBsAg 消失并产生抗HBs(适用于所有CHB 患者)。
病毒学应答(virological response,VR):对于NA治疗的患者,治疗3~6 个月后HBV DNA 测不出(应用敏感的PCR 试剂);对于IFN 治疗的患者,在治疗6 个月后和治疗结束时,HBV DNA <2000 IU/ml。
完全应答:治疗结束后病毒学应答且在长期随访过程中出现持续HBsAg 消失。
治疗结束后持续病毒学应答(sustained off-treatment virological response,SVR):治疗结束后病毒学应答至少持续12 个月。
维持病毒学应答:长期抗病毒治疗的情况下,HBV DNA 测不出。
部分病毒学应答:应用NA 治疗至少半年以上,HBV DNA 下降超过1 log10 IU/ml,但仍然可以测出。
原发无应答:治疗3 个月后,HBV DNA 较基线下降小于1 log10 IU/ml。
病毒学突破:在治疗过程中HBV DNA 水平上升超过1 log10 IU/ml,通常是由于患者的依从性差,或出现HBV 耐药所致。
组织学炎症坏死程度评估还没有作为一个标准用于儿童的临床研究来评价对治疗的应答。
治疗人群及治疗时机
治疗的决策必须要考虑到以下内容:在儿童时期疾病进展缓慢;未来出现疾病进展的风险;在目前还不能很好确定的极少数患儿中发生严重的并发症;目前抗病毒药物的有效性及副作用;目前批准的能应用于儿童的药物非常有限等。图1 为治疗流程图。
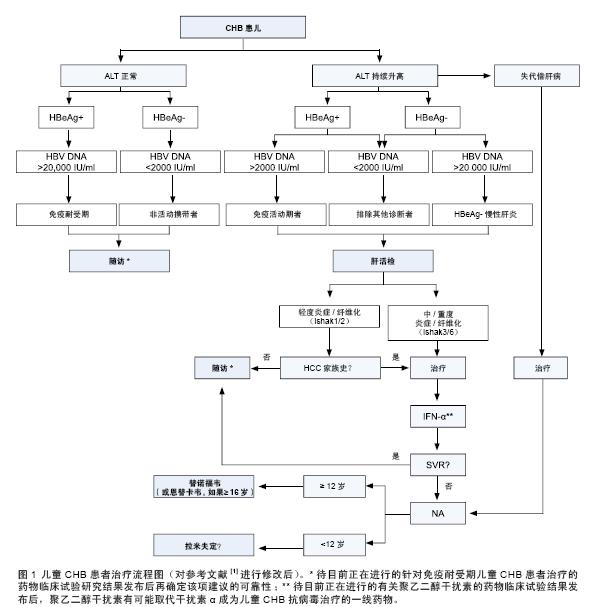
患儿每次随访时都应评价是否需要抗病毒治疗,以便在发现肝损伤的最早期征象时开始抗病毒治疗(C2)。CHB 患儿应每6 个月进行一次体格检查,检测血清ALT和HBeAg/ 抗HBe 水平(C1)。HBeAg 阳性伴ALT 持续升高的患者,上述指标应每3 个月检测一次,持续至少1 年(B1)。
HBeAg 阴性的患者,在第一年应每4 个月检测血清ALT 和HBV DNA 水平,以排除HBeAg 阴性肝炎。如果已确定为非活动携带者(ALT 正常,HBVDNA<2000 IU/ml),应每6 个月检查一次(B1)。每年检测一次全血细胞计数和肝功能(C1)。依据患者肝纤维化的分级,应用超声波筛查HCC,每6~12 个月进行一次。甲胎蛋白(alpha-fetoprotein,AFP)虽然应用广泛,但近来发现对于HCC 的有效监测敏感性和特异性不足。即便是对于非活动携带者,终生随访也是必要的,因为肝硬化、HCC 和HBV 感染的再激活,伴有HBeAg 阳性的逆转或进展为HBeAg 阴性乙肝等风险始终存在(C1)。
儿童ALT 水平正常值上限(Upper Limit of Normal,ULN)目前还没有确定。如果ALT 水平> 实验室ULN的1.5 倍或>60 IU/ml(这个值在3 个最大的儿童药物临床试验中被用作纳入标准),建议考虑抗病毒治疗,以先达到者为准(C2)。氨基转移酶较低的患者获得血清学应答的机会较少。在将来的研究中可以使用较低的ALT 阈值(该阈值来源于较大的儿童队列),以避免低估肝脏损伤。但这个新方法有可能降低总体血清学应答率,使需要长期应用抗病毒药物以维持病毒学应答的患儿增加。
患儿的ALT 水平升高至少6 个月(HBeAg 阴性者超过12 个月)时,应考虑抗病毒治疗,这样可以避免给予正在自发HBeAg 血清学转换的患儿不必要的治疗(C1)。出现血清ALT 升高时,检测血清HBV DNA 的水平非常重要,因为高水平HBV DNA 需要抗病毒治疗,而低水平HBV DNA 则应当排除其他原因的肝病。儿童的HBV DNA 水平临界值还未确定。
由于年轻患者的HBV 复制程度高于成年人,许多研究者选择了20 000IU/ml。但是,低的HBV DNA 在成年人也伴随有肝病的进展。因此,最新的成人慢性乙肝诊疗指南确定2000 IU/ml 作为一个比较可靠的临界值。这个值显然也可应用于儿童(C1)。
对于40 岁以上的患者,仅有高病毒载量就可以启动抗病毒治疗,因为高病毒载量是肝硬化和HCC 的独立危险因素。但在儿童中没有资料支持这一观点。由于目前能应用于儿童的抗病毒药物对于特殊人群只有部分或有限的应答,因此建议在考虑治疗之前进行肝组织学检查,以评估肝脏的炎症程度及肝纤维化分期(A1)。肝组织学显示至少中度炎症坏死或中度纤维化的患儿更有可能对干扰素α 和NA 都产生治疗应答(A1)。
尽管目前还不能确定轻度炎症坏死或纤维化的患儿能否从治疗中获益,但如果有HCC 家族史,即使患儿仅有轻度组织学改变,也应该进行抗病毒治疗,因为他们并发HCC 的风险增高(B2)。目前虽然还没有得到充分肯定,但应用非侵入性的方法例如FibroScan 评价肝纤维化程度,已被证明在替代肝活检方面是有用的,尤其是在随访过程中。
但是,在儿童中还没有得到足够的数据。而且目前这些非侵入性的方法在判断是否对一个CHB 儿童或青少年进行治疗方面还不能取代肝活检,因为这些方法评估的主要是肝纤维化的程度,而不是肝脏炎症坏死(C2)。
接受肝移植的HBV 感染患儿或接受抗HBc 阳性供者的患儿,都应当接受NA 抗病毒治疗,以防止(或治疗)HBV 感染的再发。准备接受免疫抑制治疗或细胞毒性药物治疗的HBsAg 阳性患者也应该接受预防性抗病毒治疗。因为这样可以减少由于乙肝再活动导致的死亡或发病的风险(B1)。
已发展至肝硬化、乙肝相关性肾小球肾炎、或合并感染HDV、HCV、HIV 的患儿,其肝病快速进展的风险增高。在这种情况下,即使血清ALT、HBV DNA 及肝组织学未满足上述的抗病毒治疗标准,抗病毒治疗也可使患者受益(C2)。
处于免疫耐受期的儿童,不应当进行抗病毒治疗,但应当监测。而在出现ALT 升高、提示免疫激活时,再进行抗病毒治疗(A1)。
现有抗病毒药物的有效性
美国食品药品管理局(Food and Drug Administration,FDA)已批准5 种药物可用于治疗儿童CHB :干扰素α、拉米夫定、阿德福韦酯、恩替卡韦及最近批准的替诺福韦。干扰素α 可用于12 个月以上儿童,拉米夫定可用于3 岁以上儿童,阿德福韦酯和替诺福韦可用于12 岁及以上儿童,恩替卡韦可用于16 岁以上患者。这些药物都有优缺点(表2)。迄今为止,上述药物无一得到欧洲药品管理局批准用于儿童。
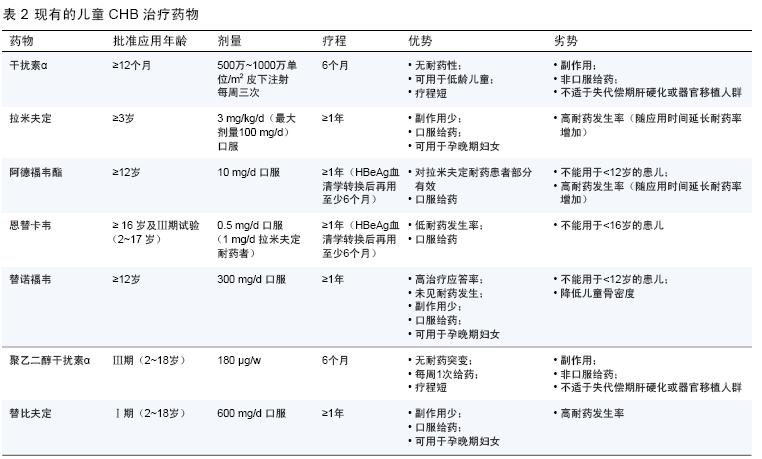
治疗应答的预测因素
干扰素α 和拉米夫定治疗的儿童中已确定了若干个基线和治疗中的应答预测因素,而其他NA 尚无儿童研究数据。HBeAg 阳性患者对干扰素α 的应答与以下因素有关:治疗前低病毒载量及高水平ALT(超过2 倍ULN)、年轻及女性(A1)。基线ALT 高水平患者与停药后更高的持久血清学转换率相关(B2)。
对干扰素α 早期应答的患者较之延迟应答和无应答患者,更容易出现HBsAg 消失(C2)。在成年患者,病毒基因A 型和B型较之C 型和D 型患者,对干扰素α 的应答更好。
目前还没有关于儿童病毒基因型对抗病毒治疗应答影响的相关研究。因此在确定病毒基因型是否会影响到儿童CHB 治疗的选择及是否可以预测治疗应答之前,目前不推荐在抗病毒治疗开始前检测病毒基因型(C2)。基线高ALT 水平(至少是ULN 的2 倍)、高组织学活动度指数的患儿,拉米夫定治疗更容易获得应答(A1)。
治疗策略
目前对于HBeAg 阳性伴ALT 水平升高的患儿,有限疗程的干扰素α 抗病毒治疗仍是治疗策略的首要选择(A1),因为这部分患者人群主要的治疗目标是HBsAg 的血清学转换。干扰素α是目前唯一可用的能使患者停药后持续应答的药物。一旦聚乙二醇干扰素治疗儿童CHB的临床试验结果发布,聚乙二醇干扰素很可能将会成为推荐药物。虽然干扰素α 有较大的副反应且其长期获益有待进一步确定,但应用干扰素不会出现相关的基因耐药。推荐方案是5 百万~1 千万单位/平方米体表面积,每周3 次,疗程6 个月(A1)。
干扰素α 在儿童中的禁忌证包括肝硬化失代偿期、血细胞减少、自身免疫性疾病、心脏和肾脏功能衰竭以及接受器官移植(B1)。应用糖皮质激素诱导治疗能否使患者获益还没有被证实(C2)。无论在成人还是儿童中,干扰素α 与拉米夫定联用治疗的应答率均高于单用干扰素α,但停药后的应答率未见优势。因此目前不推荐联合治疗(C2)。
干扰素α 是唯一获准用于3 岁以下患儿的药物,而这些患儿罕有需要治疗的(A1)。对于该年龄段,应考虑干扰素相关的神经毒性(尽管多数属轻度或一过性)。如果干扰素α 治疗无应答,在考虑其他治疗前也应当先观察6~12 个月,因为有的患儿在停用干扰素α 治疗6 个月内还有可能获得VR(B1)。
对于12 岁以上患者,替诺福韦(或恩替卡韦对于≥ 16 岁的患者)将是最佳选择,因为其病毒应答率高,耐药率低(A1)。替诺福韦的推荐剂量是300 mg/ 天,恩替卡韦的推荐剂量是0.5 mg/ 天(对于初治患者)(A1)。尽管替诺福韦还未获批准用于治疗12 岁以下CHB 患者,但对这部分患儿也应该是安全的,因为替诺福韦已广泛应用于(获得FDA 批准)2 岁以上HIV 感染者。一项2~11 岁CHB的3 期临床试验正在进行中。因为替诺福韦已获准用于青少年,就不再推荐阿德福韦酯,原因是耐药风险较高、应答率较低(B1)。
如果在治疗过程中获得HBeAg 血清学转换,替诺福韦或恩替卡韦的治疗也可成为有限疗程(C2)。NA 治疗的疗程还未确定,但在达到HBV DNA 测不出和HBeAg血清学转换后还应至少再治疗12 个月(B1)。由于有相当一部分成年患者在停止治疗后不能维持血清学和病毒学应答,因此对于组织学证实肝纤维化较严重的患者,更安全的选择是将治疗的疗程延长至HBsAg 消失(C2)。在停止治疗后应加强监测,因为有可能出现停药后的肝炎活动(B1)。
治疗中未出现HBeAg 血清学转换者、罕见的HBeAg 阴性CHB 及肝硬化患儿均需NA 长期治疗(B1)。若年龄允许,替诺福韦或恩替卡韦为首选(A1)。成人长期有效性和安全性数据支持该策略,但迄今尚无青少年数据。NA 长期治疗中,应每3 个月检测一次HBV DNA,因为将HBV DNA 降低至测不出的水平对于避免耐药至关重要(B1)。
拉米夫定应当限制在以下少见的几类患儿使用:对干扰素α 治疗无应答、需要快速抑制病毒及其他特殊人群(见下文)等(C1)。推荐的拉米夫定治疗剂量为3 mg/kg/d(最大剂量100 mg/d),口服,每天1 次(A1)。最佳疗程难以确定,应当持续治疗直到获得VR,在获得HBeAg 血清学转换后可能需要再治疗12 个月(B1)。由于治疗时间越长,耐药风险越大,因此建议如果治疗6 个月没有获得完全病毒学抑制或出现耐药突变,应停用拉米夫定(B1)。停药后ALT 可能升高,建议患儿在停药后密切监测。对于病情严重和ALT显著升高的患儿,应再次服用拉米夫定(对于未出现拉米夫定耐药的患者)或换药(若年龄允许,可用替诺福韦)(A1)。肝硬化患儿需长期抗病毒治疗,可换用替诺福韦(≥ 12 岁时)单用或联合恩替卡韦(≥ 16 岁时),也可维持拉米夫定(<12 岁时),尽管是不完全VR,也如此推荐(C2)。
干扰素α 与拉米夫定联合治疗前景很好,但需要更多的儿童患者数据(C2)。阿德福韦酯与拉米夫定联用仅在阿德福韦酯单药治疗无应答患者中进行试验,其疗效还未与单药治疗进行比较。
尽管还没有来自儿童研究的数据,但目前成人的诊治指南建议HBeAg 阴性患者如果持续ALT 升高(在12个月内至少检测到3 次升高)且HBV DNA 高水平时,应当考虑采用与HBeAg 阳性患者同样的抗病毒治疗流程(C1)。但应特别注意这类患者有更高的复发率,需要治疗更长时间。
治疗失败和抗病毒耐药
对NA 治疗部分应答或原发性无应答常常与基因耐药株病毒的出现或患者的依从性较差有关。无应答患者应进行HBV 基因序列分析以鉴别耐药或依从性差(C1)。在青少年患者,依从性差可能是主要问题,特别是在需要长期治疗以获得维持性应答的患者。
在应答患者,病毒学突破(随后可能会出现生化学突破)通常继发于病毒耐药。出现病毒学突破的可能性决定于NA 药物内在的耐药屏障作用(耐药性拉米夫定> 替比夫定> 阿德福韦酯> 恩替卡韦> 替诺福韦)。所有NA 治疗患儿都应通过每3 个月检测一次HBV DNA来发现病毒学突破(C1)。理想状态下,应及早确定病毒学突破,并在ALT 升高前更改治疗方案。由于批准可用于儿童的有效药物很少,因此当儿童出现对某种NA的耐药时,应基于患者肝穿活检及年龄调整治疗方案。
如果是轻度肝损伤,患者可换用恩替卡韦(用于阿德福韦酯耐药,≥ 16 岁且拉米夫定初治的患者)或替诺福韦(用于≥ 12 岁,拉米夫定耐药或拉米夫定经治又出现阿德福韦酯耐药的患者)(C2)。对于低龄儿童,目前除了拉米夫定以外没有其他NA 批准应用,可以换用干扰素α(当聚乙二醇干扰素获得批准时,也可应用)(C2)。若患儿在治疗后出现病情加重,应停用拉米夫定,并密切随访(C2)。对于中度肝损伤/ 肝纤维化的患者,如果≥ 12 岁,应换用替诺福韦;如果在12 岁以下,换用干扰素α(C2)。
如果肝活检发现重度肝损伤,换用替诺福韦是唯一可行的选择(可单用,如果患者≥ 16 岁且高病毒载量时可与恩替卡韦联合应用)(C2)。替诺福韦和恩替卡韦对拉米夫定耐药患者都有效,但这类人群换用恩替卡韦后耐药增加(治疗2 年后耐药的发生率8%),需要应用大剂量(1 mg/d)(B1)。换用恩替卡韦后应停用拉米夫定,以减少耐药突变的风险(C2)。替诺福韦可用于拉米夫定耐药突变株病毒,因为替诺福韦的活性不受耐药株影响(B1)。
对于治疗24 周(应用拉米夫定患者)或48 周(应用阿德福韦酯患者)仅获得部分病毒学应答的患者,若年龄允许,建议换用替诺福韦或恩替卡韦(B1)。对于12岁以下患儿,难以确定治疗策略。如果既往未用过干扰素α 的可换用干扰素α(或聚乙二醇干扰素),或继续拉米夫定治疗直至达到12 岁(对于严重肝纤维化或肝硬化患者,这是唯一的选择)或停用拉米夫定治疗,停药后合理随访(C2)。
由于耐药突变株正逐渐成为一个严重的公共卫生问题,因此如果应用这些已批准的药物不太可能获益,建议儿科医生先不给予抗病毒治疗,可考虑等待更有效的药物上市(C1)。
下一篇:如何在临床实践中遵循慢乙肝防治指南?