抗乙肝病毒核苷(酸)类似物的不良反应
来源:中国医学论坛报 作者:北京地坛医院 蔡皓东
抗乙肝病毒核苷(酸)类似物的不良反应(一)
最近十年,口服核苷(酸)类似物的应用使乙型肝炎治疗取得重大进展。拉米夫定、阿德福韦酯、恩替卡韦、替比夫定和替诺福韦5种药物已被批准用于治疗慢性乙型肝炎,其中前4种已在我国上市,替诺福韦也将在我国开展临床试验。
虽然药物获批程序非常严格,但某些发生率很低或在长期用药期间发生的不良反应仍可能被临床前试验和临床试验疏漏或忽视。上述可能的不良反应仍须关注,因为多数应用核苷(酸)类似物的乙型肝炎患者须接受长期治疗,至少治疗4~5年,部分患者甚至须终生治疗。
近日,国家食品药品监督管理局(SFDA)发布第30期《药品不良反应信息通报》(以下简称《通报》),提醒医师警惕治疗乙型肝炎的核苷(酸)类抗病毒药替比夫定和拉米夫定的横纹肌溶解症。《通报》发布后,该类药物引起的不良反应受到广泛关注。笔者对抗乙型肝炎病毒(HBV)核苷(酸)类似物引起的不良反应作一综述,供临床医师参考。
核苷(酸)类似物与DNA聚合酶
目前,所有口服抗HBV核苷(酸)类似物的药理作用均为通过与HBV DNA聚合酶底物竞争以抑制DNA聚合酶,从而阻止HBV DNA复制。药物在抑制病毒DNA聚合酶的同时,也可能对人体的DNA复制产生影响。人类真核细胞包括5种DNA聚合酶,分别为α、β、γ、δ和ε。其中,DNA聚合酶α、β、δ和ε均位于细胞核内,参与细胞DNA的复制和修复,而DNA聚合酶γ则存在于线粒体并参与线粒体复制,也被称为线粒体DNA(mtDNA)聚合酶。
mtDNA聚合酶损伤可能导致线粒体疾病。虽然氟碘阿糖胞苷对病毒的抑制作用很强,但对人类细胞线粒体亦有毒性作用,应用该药9~13周可诱发以乳酸酸中毒、肝衰竭、胰腺炎、肌病为主要表现的线粒体中毒综合征。最典型事件是上世纪90年代初期的氟碘阿糖胞苷临床试验,在接受氟碘阿糖胞苷治疗的15例患者中,有5例死于肝衰竭,因此该药临床试验被终止。
目前上市的核苷(酸)类似物主要作用于DNA聚合酶β和γ,而在人体细胞DNA合成中起主要作用的为DNA聚合酶α和δ;且药物对人类DNA聚合酶β的抑制作用很弱,仅对人类DNA聚合酶γ有低水平抑制作用。因此,目前上市的核苷(酸)类似物通常不影响人类DNA复制和修复。但由于乙型肝炎治疗的长期性,该类药物仍可能对人细胞DNA聚合酶γ产生一定的毒性作用。
核苷(酸)类似物产生线粒体毒性的机制
线粒体的生命周期有限,平均寿命约为10天,具有较高的更新率,因此须不断复制。线粒体是一种半自主细胞器,既依赖核DNA(nDNA)编码、复制、转录和翻译,也有自己的蛋白质合成系统,可通过自身的DNA聚合酶自我合成。由于在线粒体复制过程中,mtDNA呈裸露状态,无组蛋白保护,易受到侵害;同时,线粒体内缺乏较有效的修复系统,在复制时有不对称状态,出现的单链DNA有自发脱氨基作用,因此更易发生突变。
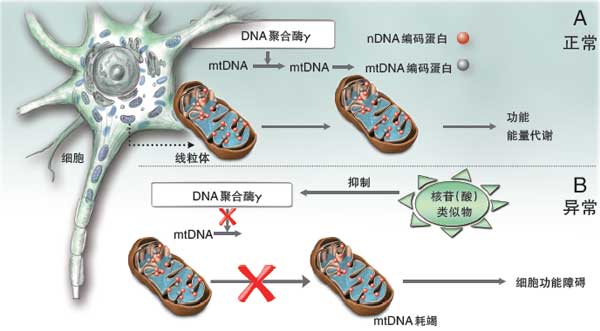
长期应用核苷(酸)类似物治疗可能对mtDNA聚合酶产生一定的抑制作用,导致细胞内mtDNA异常,其含量减少甚至耗竭(图1)。线粒体是细胞内氧化磷酸化和形成三磷酸腺苷(ATP)的主要场所,也是调控细胞凋亡和活性氧产生的重要部位。当线粒体异常或减少达一定程度时即可影响其氧化磷酸化功能,使ATP生成减少,出现细胞功能障碍或细胞凋亡。在体外试验中,许多抗HBV核苷(酸)类似物在高于人类治疗剂量10~100倍时可表现出线粒体毒性。
图1 核苷(酸)类似物相关线粒体毒性的发生机制 A:线粒体内发生氧化磷酸化和能量代谢时须nDNA和mtDNA编码的蛋白参与。 B:当细胞内的核苷(酸)类似物浓度超过标准阈值时,人类DNA聚合酶γ活性可能被抑制。如人类DNA聚合酶γ活性受抑制持续时间较长,细胞内mtDNA水平可能会由于复制受损而降低。由于缺少与呼吸链相关的蛋白,且活性氧生成增多引起细胞内蛋白质、脂质和mtDNA进一步损伤,导致线粒体功能异常。
药物所致的常见线粒体疾病
人体细胞中有几百甚至几千个线粒体,平均每个细胞内有300~400个线粒体。但线粒体在不同细胞中分布不一致,线粒体常集中分布于代谢活跃部位,如肌肉、心肌、神经、肝脏、肾脏、胰腺等组织的细胞中线粒体数量较多,因为这些组织须较多ATP供应能量。另外,线粒体亦较常分布于有较多氧化反应底物的部位,例如脂肪滴,因为脂肪滴中含许多须被氧化的脂肪。因此,该类药物所致的线粒体损害可能导致以下疾病发生:肌病、肾小管病、周围神经病、肝衰竭、乳酸酸中毒、心肌病和胰腺炎等。
不同的核苷(酸)类似物可能导致不同部位的线粒体损伤。阿德福韦酯和替诺福韦均具有潜在的肾毒性,可引起肾小管病。替比夫定可能导致肌病和周围神经病,与干扰素联合应用时,患者发生周围神经病的风险明显升高。终末期肝病模型(MELD)评分高的肝硬化患者在接受恩替卡韦治疗时,有发生乳酸酸中毒的风险。另外,目前还有部分可疑为线粒体损害的个案报道,如拉米夫定引起横纹肌溶解,阿德福韦酯引起胰腺炎,恩替卡韦引起周围神经病等。[1910401]
■编后
我国是一个慢性乙型肝炎患者众多的国家,其治疗被医师和患者所关注,尤其是长期治疗的安全性更是关注的焦点。目前文献报告的抗乙肝病毒核苷(酸)类似物所致的不良反应主要包括肾小管病、肌病、周围神经病和乳酸酸中毒等,分别具有如下特点:
1.肾小管病 主要见于阿德福韦酯和替诺福韦,其肾毒性均与药物剂量相关。
2. 肌病 在应用核苷(酸)类似物治疗乙型肝炎的过程中,导致肌病的药物主要为替比夫定,亦有 拉米夫定引起肌病的个案报道。
3. 周围神经病 主要见于替比夫定与干扰素联合治疗,亦有恩替卡韦引起周围神经病的个案报道。
4. 乳酸酸中毒 核苷(酸)类似物相关的乳酸酸中毒既往主要见于艾滋病治疗,在抗HBV治疗中 仅见个案报道,我国未见相关报道。
抗乙肝病毒核苷(酸)类似物的不良反应(二)
--肾小管病概述及案例分享
概述
肾毒性与药物剂量相关
核苷(酸)类似物导致的肾小管病主要见于阿德福韦酯和替诺福韦,二者肾毒性与药物剂量相关。
当阿德福韦酯剂量大于30 mg/d时,肾毒性发生率为22%~50%。一项治疗慢性乙型肝炎的临床试验对患者予阿德福韦酯30 mg/d、10 mg/d或安慰剂治疗48周,结果为,在应用阿德福韦酯30 mg/d的患者中,有8%出现肾损害,而阿德福韦酯10 mg/d的安全性与安慰剂相近,且仍有明显抗乙型肝炎病毒(HBV)活性。因此,目前阿德福韦酯被批准用于治疗慢性乙型肝炎的剂量为10 mg/d。长期应用阿德福韦酯10 mg/d的肾毒性很低,在既往无肾病的患者中,应用阿德福韦酯1年的肾毒性发生率为0,应用5年的发生率为3%~8%。对于等待肝移植或肝移植后的患者,虽然通常应用环孢素、他克莫司等有肾毒性的药物,但在接受阿德福韦酯10 mg/d治疗1~3年后,仅4%的患者因肾毒性而中断治疗。甚至肾移植、肾透析及肾功能不全患者在根据血清肌酐清除率调整药物剂量后,亦对阿德福韦酯有较好的耐受性。
关于替诺福韦的动物试验显示,短尾猴免疫缺陷病毒感染模型在长期应用替诺福韦时会出现剂量依赖性的肾小管毒性。替诺福韦的肾毒性主要见于艾滋病治疗中,其发生率为4%~6%。在慢性乙型肝炎治疗中,替诺福韦的肾毒性发生率显著低于阿德福韦酯。在慢性乙型肝炎患者接受核苷(酸)类似物治疗的48周期间,在替诺福韦组(300 mg/d,426例)没有患者的血肌酐较基线升高≥0.5 mg/dl,在阿德福韦酯组(10 mg/d,215例)有1例(0.5%)。
发病机制
除线粒体毒性外,阿德福韦酯和替诺福韦相关肾小管病的发病机制还与人有机阴离子转运蛋白-1(hOAT-1)对药物的聚集作用有关。
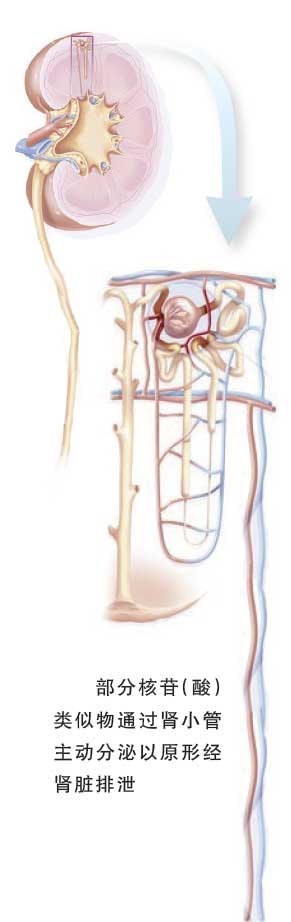
阿德福韦酯和替诺福韦这2种药物均通过肾小管主动分泌的方式以原形经肾脏排泄。有研究显示,hOAT-1对阿德福韦酯有较强的亲和力,可主动摄取阿德福韦酯,使其在肾脏近曲小管周围有较高的药物浓度。在替诺福韦相关肾损害的患者中,亦存在这种现象。肾小管周围较高浓度的药物可能抑制肾脏近曲小管细胞的mtDNA聚合酶,使线粒体肿大、变形,mtDNA的数量明显减少,从而影响肾小管的重吸收(尤其是肾小管对磷的重吸收)和分泌功能,严重时可导致肾小管细胞凋亡。
临床表现及预防
在治疗慢性乙型肝炎的过程中,肾小管病临床表现通常较轻微,仅出现血肌酐轻度升高和无症状的血磷降低,在停药或减小剂量后即可消失。典型和重症肾小管病罕见,多见于艾滋病治疗,或与用药过量和其他危险因素相关,主要表现为肾性电解质紊乱、肾小管性酸中毒、肾性低血磷及骨质疏松、凡科尼(Fanconi)综合征、急性肾小管坏死和急性肾衰竭。
患者接受阿德福韦酯和替诺福韦治疗期间,应尽量避免联用其他有肾毒性的药物,定期复查肾功能和血磷,计算并根据肌酐清除率调整药物剂量,必要时更换治疗方案。
典型病例
病史简介
患者男,40岁,身高161 cm,体重70 kg,因慢性乙型肝炎自2004年2月于我院门诊接受治疗。既往无肾脏病史。
患者1980年发现有HBV感染,肝功能正常。1996年因肝功能异常入院治疗,接受干扰素治疗3个月后因不能耐受不良反应而停药。2000年5月,开始服用拉米夫定(100 mg/d),2003年10月因对拉米夫定耐药而自行停药,其后肝功能再次异常。2004年2月~2005年2月再次服用拉米夫定,因耐药而再次停药。
2006年12月,患者于我院复查。血液检查:丙氨酸氨基转移酶(ALT)140.9 U/L,天冬氨酸氨基转移酶(AST)89.3 U/L,总胆红素(TBIL)10.2 μmol/L,肌酐(Cr)98 μmol/L,尿素氮(BUN)7.26 mmol/L,空腹血糖4.94 mmol/L,血磷0.98 mmol/L,血钙2.59 mmol/L,其他生化检测指标均正常。尿常规指标正常。HBsAg、HBeAg和HBcAb阳性,HBV DNA 1.77×105 copies/ml。
2006年12月,患者开始服用阿德福韦酯(10 mg/d)。每3个月随访1次,行肝肾功能及乙肝病毒学检测。患者治疗依从性好,3个月后肝功能恢复正常,6个月后HBV DNA<500 copies/ml。9个月时,患者Cr升高至124 μmol/L,BUN 7.13 mmol/L,血磷正常,尿量正常,全身无水肿,计算其肌酐清除率为68.9 ml/min,继续按原剂量应用阿德福韦酯。其后肝功能正常,HBV DNA持续为检测下限(<500 copies/ml),BUN 7.13~9.83 mmol/L,Cr 124~130 μmol/L,血磷0.76~0.91 mmol/L。治疗第2年9个月时,检测其Cr升高至166 μmol/L,BUN 9.46 mmol/L,血磷0.69 mmol/L,尿蛋白(-),计算肌酐清除率为49.9 ml/min,阿德福韦酯减量至10 mg qod。药物减量6周后复查,Cr 114 μmol/L,BUN 7.09 mmol/L,血磷0.86 mmol/L。其后患者持续服用阿德福韦酯10 mg qod,目前已随访半年余,HBV DNA维持于检测下限,肝肾功能及血磷均正常。
病例分析
本例患者既往曾应用拉米夫定,且已发生耐药,改用阿德福韦酯治疗后HBV DNA下降至检测下限。
目前对拉米夫定耐药患者的治疗包括以下几种:① 换用或加用阿德福韦酯或替诺福韦;② 停用拉米夫定,改用恩曲他滨+替诺福韦;③ 换用恩替卡韦。替诺福韦及含恩曲他滨+替诺福韦的复方制剂在我国尚未上市,而拉米夫定耐药的患者对恩替卡韦的耐药率仍较高(治疗4年后的耐药发生率达43%),已不建议应用。
本例患者在对拉米夫定耐药后换用阿德福韦酯,治疗效果良好,一直维持病毒学应答,因此,依据患者肌酐清除率将阿德福韦酯的剂量调整为10 mg qod。减小阿德福韦酯剂量可降低其对肾小管的毒性,且由于患者肌酐清除率下降,减小药物剂量仍可达到有效血药浓度,维持病毒学应答。
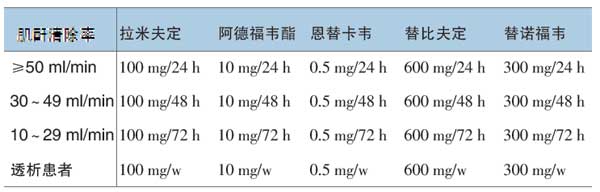
本例提示,对乙型肝炎患者,在阿德福韦酯治疗过程中出现肾损害时,如不能改变治疗药物,可通过减小剂量而继续治疗(参照下表),仍可达一定治疗效果。
表 肌酐清除率与核苷(酸)类似物治疗慢性乙型肝炎的剂量
抗乙肝病毒核苷(酸)类似物的不良反应(三)--肌病概述及案例分享
概述
发病情况
肌病的发生与许多核苷(酸)类似物有关,目前关于抗艾滋病药物齐多夫定所致肌病的病例报告较多。在乙型肝炎的治疗过程中,肌病这一不良反应主要见于替比夫定,亦有拉米夫定引起肌病的个案报道。此外,另一核苷(酸)类似物克来夫定被发现可引起严重肌病,因此2009年4月在美国被终止其Ⅲ期临床试验。
作为核苷(酸)类似物,替比夫定于2006年被批准用于治疗慢性乙型肝炎,剂量为600 mg/d。替比夫定导致的肌病较少见。有研究报告,在接受替比夫定治疗4年的乙型肝炎患者中,肌肉症状的发生率为3.1%(20/655例),肌病(或肌炎)发生率为0.9%(6/655例)。
临床特点
目前关于替比夫定相关肌病发生机制的研究较少,尽管研究者在体外试验中未发现其线粒体毒性,但尚不能排除在临床应用中替比夫定相关线粒体毒性的可能性。
替比夫定相关肌病的临床症状通常较轻微,主要表现为肌痛、肌无力和肌酸激酶(CK)水平升高。通常首先发生CK水平升高,在1~6个月后出现肌痛、肌无力症状。在发生肌病时,患者常伴血清天冬氨酸氨基转移酶(AST)水平异常。多数患者转归较好,在停药2~4周后CK水平明显降低,症状亦随之改善。但病情如未得到及时处理,则可能进展为横纹肌溶解。
预防及治疗
在应用替比夫定前,医师应询问患者有无甲状腺疾病史、肌病史或肌病家族史,有无须治疗的严重高脂血症等疾病史。对有以上病史的患者,应尽可能不选择应用替比夫定,尽量避免与其他可能导致肌病的药物联合应用。
在应用替比夫定治疗期间,医师应注意对患者CK水平进行监测,但与应用替比夫定相关的CK水平升高3~4级较常见。GLOBE试验104周的数据显示,在接受替比夫定治疗的患者中,CK水平升高3~4级者占12.9%,但多为无症状、单发和一过性的,通常不影响治疗。因此,医师仅根据出现3~4级CK水平升高尚不能判定肌病发生,须结合患者临床表现、肌电图检查和肌肉活检结果等进行综合判断。
有CK水平持续升高和(或)可疑肌病的患者,除停用替比夫定外,还应注意休息,通常无须特殊治疗。患者在停药4~8周后CK水平即可恢复正常,其后肌肉症状亦逐渐恢复。对于肌肉症状严重或停药后恢复较慢的患者,可选择应用辅酶Q10治疗。
典型病例
病史简介
患者男性,24岁,7年前体检时发现有乙肝病毒(HBV)感染,曾应用干扰素治疗,但数月后因无法耐受药物副作用而停药。
2007年10月,患者出现肝功能异常,开始服用拉米夫定。7个月后,肝功能恢复正常,HBV DNA最低降至2.34×103 copies/ml。自2008年5月起,改用阿德福韦酯治疗。10个月后复查丙氨酸氨基转移酶(ALT)44 U/L,HBV DNA 5×104 copies/ml,改为替比夫定600 mg/d治疗。3个月后查肝功能恢复正常,HBV DNA<500 copies/ml。
2009年9月,患者复查CK>300 U/L(正常值38~174 U/L)。2个月后,在打篮球等剧烈运动时自觉无力,其后渐感觉爬楼梯时肢体无力。复查CK水平异常,未停药。1个月后渐出现心慌,小跑20米后自觉心跳加速、无力,无法正常抬腿。其后渐有肌肉疼痛,活动时加重,有下肢水肿,下蹲后起立困难,但可走平路,腹部、胸部、背部及四肢近端肌肉无力,伴疼痛。患者自发病后尿色无改变。
2009年12月,患者于我院复查,ALT 32.1 U/L,AST 64.7 U/L,CK 1614 U/L,肌酸激酶同工酶(CK-MB)30 U/L(正常值<25 U/L),乳酸脱氢酶(LDH) 293 U/L(正常值80~285 U/L),α-羟丁酸脱氢酶(HBDH) 322 U/L(正常值74~182 U/L),HBV DNA<500 copies/ml。
医师考虑本例症状与应用替比夫定有关,故改用拉米夫定+阿德福韦酯联合治疗。20天后,患者肌痛、心慌症状未减轻,下肢水肿加重。查AST 56.4 U/L,CK 1252 U/L,CK-MB 43 U/L,LDH 315 U/L,HBDH 385 U/L,血电解质及肾功能正常,血、尿、大便常规正常。患者以“肌痛原因待查、可疑横纹肌溶解”入住我院。
体格检查:神清,颅神经(-),低头转颈无力,双侧三角肌、肱二头肌肌力Ⅳ级,左侧肱三头肌肌力Ⅲ级、右侧Ⅳ级,双侧上肢远端肌力Ⅴ级,双侧股四头肌肌力Ⅲ级,双侧下肢远端肌力Ⅳ级。四肢腱反射减弱,无明显感觉障碍,双侧肱二头肌、肱三头肌、股四头肌及右侧胸大肌有压痛,全身肌肉无萎缩。双侧病理征(-)。血气分析:pH 7.345,氧分压(PO2)15.18 kPa,二氧化碳分压(PCO2)4.44 kPa,氧饱和度98.3%,碳酸氢根浓度17.7 mmol/L,剩余碱 -7.0,考虑代谢性酸中毒、乳酸酸中毒可能性大。肌红蛋白及肌钙蛋白正常。心电图提示为窦性心动过速,心率117 次/分。
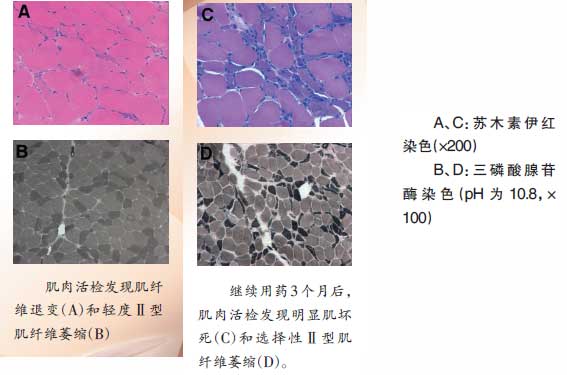
患者接受利尿剂(呋塞米和螺内酯)、辅酶Q10、维生素C、维生素B1、维生素B12、果糖二磷酸钠治疗,下肢水肿迅速消退,心率64~80 次/分,心慌症状好转。1周后,行左侧肱三头肌肌肉活检,病理检查见肌组织纤维变性、坏死、吞噬,有大量再生肌纤维,部分空泡化,部分肌纤维内有嗜伊红染色的胞浆体,符合坏死性肌病病理改变。
病例分析
患者曾应用干扰素、拉米夫定和阿德福韦酯,均未达病毒学完全应答。改用替比夫定后,HBV DNA降至检测值下限,肝功能恢复正常。但治疗8个月后出现肌痛和肌无力,CK>正常值上限5倍,多处肌肉压痛,肌力减退,无感觉异常和肌萎缩。左侧肱三头肌肌肉活检诊断为坏死性肌病。停用替比夫定后CK水平渐降低,肌痛减轻,肌力渐恢复。因此,本例可确诊为替比夫定所致坏死性肌炎。
临床试验数据显示,在接受替比夫定治疗2~4年的患者中,肌病或肌炎发生率为0.3%~0.9%。多数患者转归较好,停药2~4周后CK水平明显下降,症状改善,但处理不及时则可能进展为横纹肌溶解,出现乳酸酸中毒和肾衰竭。
横纹肌溶解是由于骨骼肌细胞严重损伤和死亡导致的疾病。患者可有剧烈肌痛、肌肉压痛、肌肉肿胀及肌无力,血清CK水平超过正常值上限10倍以上,有时可达正常值2000倍或更高。尿液呈红褐色,尿肌红蛋白>1 mg/L,常并发乳酸酸中毒和急性肾衰竭。本病预后差,患者病死率高。本例患者有轻度酸中毒,但肌红蛋白和肌钙蛋白水平正常,因此尚不能诊断为横纹肌溶解。
本例提示,在应用替比夫定治疗乙型肝炎的过程中,应注意监测患者CK水平,询问其肌肉症状。如血清CK水平升高大于正常值上限5倍,且伴肌肉症状,则应考虑替比夫定导致肌病的可能,须及时停药或改变治疗方案。
链接
对应用克莱夫定后出现肌病的患者行肌活检,发现明显病理学改变。见《肝脏病学》[Hepatology 2009,49(6):2080]。
下一篇:乙肝抗病毒治疗效果的评估与监测