恩替卡韦强效、低耐药实现慢性乙肝长期治疗策略
恩替卡韦以强效、低耐药特点实现慢性乙肝长期治疗策略
上海复旦大学附属华山医院感染科 p; 施光峰
刚刚结束的亚太肝病学会2008年会(APASL 2008)公布了恩替卡韦(ETV)几项临床研究的最新结果。R.E.V.E.A.L.-HBV研究显示HBV持续低载量(HBV DNA<104 copies/ml)也与慢性乙肝(CHB)患者肝细胞癌(HCC)的危险显著相关,提示HBV载量需要抑制得越低越好。在核苷初治患者中的全球临床研究5年耐药监测数据显示,ETV长期治疗能够保持极低耐药发生率,核苷初治患者接受ETV治疗5年累计基因型耐药率仅1.2%。
日本核苷初治患者接受0.5 mg ETV治疗3年仅1例发生基因型耐药,累计耐药发生率仅为1.7%,再次从一个侧面支持了全球临床的耐药数据。ETV的强效、高基因屏障和极低耐药发生率的特点能够实现CHB患者长期治疗的策略,为乙肝治疗开创了一个新纪元。
R.E.V.E.A.L.-HBV研究——低病毒血症仍有HCC风险,HBV DNA抑制越低越好
血清HBV DNA水平持续增高是发生HCC的强独立预测因子
中国台湾大学流行病学研究生院Chen等报道,血清HBV DNA水平升高是CHB患者发生HCC的强预测因子。在R.E.V.E.A.L.-HBV研究中,他们评估了HBV DNA水平与HCC发生危险的关系,以及与HBV DNA变化有关的基线因素。
研究包括1289例在入组时HBV DNA≥104 copies/ml并且有2次以上HBV DNA检测值的患者,对照组为2020例入组时HBV DNA<104 copies/ml的患者。HBV DNA水平的低、中、高和极高界值分别定为<300 copies/ml、300~<105 copies/ml、105~<107 copies/ml和 ≥107 copies/ml。丙氨酸氨基转移酶(ALT)水平的低、中、高界值分别为<15 U/L、15~44 U/L和≥45 U/L。研究采用多分类有序反应变量logistic回归(polytomous logistic regression)分析HBV DNA轨迹水平的影响因素,采用Cox比例风险模型分析HBV DNA轨迹分类与HCC发生危险的关系。
根据HBV DNA轨迹水平将患者分为4级:Ⅰ中到低度(148例);Ⅱ中度(380例);Ⅲ高度(542例);Ⅳ持续极高(219例)。ALT轨迹水平也分为4级:低到中、中到中、高到中和中到高。随访共计40024人-年,期间在3309例患者中有89例新发HCC病例。
研究发现,患者入组时的性别、HBeAg特征和ALT水平与HBV DNA轨迹显著相关。与对照组相比,根据HBV DNA轨迹分级发展为HCC的校正风险比分别为:Ⅰ:0.7(95%CI 0.1~5.1);Ⅱ:2.6(95%CI 1.1~6.0);Ⅲ:8.5(95%CI 4.6~15.8);Ⅳ:10.0(95%CI 4.7~20.7)。经相关因素校正后发生HCC的风险比随HBV DNA轨迹分级的升高而升高。
由此可见,血清HBV DNA水平持续增高是发生HCC的强预测因子,并独立于性别、年龄、吸烟与否、饮酒与否和ALT轨迹水平。
持续低病毒血症(<104 copies/ml)与CHB患者发生HCC危险显著相关
多个CHB治疗指南均以低病毒血症(HBV DNA<104 copies/ml)作为CHB患者处于非活动性疾病状态的标准,认为这些患者疾病进展的危险很小甚至没有。然而,这些患者疾病进展的危险并没有被正确评估。在APASL 2008年会上U. H. Iloeje等同时公布了另一项R.E.V.E.A.L.-HBV研究的最新结果,分析了低病毒载量的HBV感染患者发生HCC的危险。
本项分析包括未感染HCV的HBsAg阴性患者和没有感染HCV且基线时无肝硬化的R.E.V.E.A.L.-HBV研究亚组患者。所有HCC病例都采用现有的标准进行确诊。以基线特征(年龄、性别、饮酒和吸烟情况)和HBV DNA及ALT水平的时间变化为变量,采用Cox风险模型进行多变量校正的危险比分析,确定HCC进展的危险。
共分析了18541例HBsAg阴性患者和3584例HBsAg阳性患者,在12.1年中总计评估了267809.1人-年,共发现184例HCC患者。与HBsAg阴性患者相比,经过基线和随访特征校正后,发展为HCC的HBsAg阳性患者风险比如下:HBV DNA不可检测者为3.0 (95%CI 1.4~6.3),300~9999 copies/ml者为3.3(95%CI 1.7~6.6),1×104~99999 copies/ml者为14.4 (95%CI 8.5~24.4),1×105~999999 copies/ml者为32.0 (95%CI 19.9~51.6),≥1×106copies/ml者为30.5 (95%CI 20.1~46.2)。
结果可见,低病毒血症(HBV DNA<104 copies/ml)患者进展为HCC的危险并没有被正确评估。即使排除了基线HCV感染或肝硬化因素,HBV DNA病毒载量<104 copies/ml的CHB患者发生HCC的危险也显著高于HBsAg阴性患者。HBV DNA可检测者发生HCC的危险较HBV DNA不可检测者升高3倍以上。HBV病毒血症水平在300~9999 copies/ml的患者发生HCC的危险显著高于HBV DNA<300 copies/ml者。
临床数据不断证实——ETV初治患者耐药率极低,可保障长期持久HBV病毒抑制
全球临床研究显示,ETV初治患者5年累计基因型耐药率仅为1.2%
ETV能够强效抑制乙肝病毒,并且具有高耐药基因屏障。在核苷初治患者中,4年的分析结果表明ETV耐药发生率很低,不过在拉米夫定(LVD)治疗失效患者中ETV的耐药屏障会被降低。本次APASL 2008年会报道的ETV 5年耐药检测结果再次证实,ETV长期治疗能够保持极低的耐药发生率。
ETV 全球临床研究5年耐药监测的患者群体包括核苷初治患者和LVD失效患者。核苷初治患者入组的是ETV-022研究中HBeAg阳性患者和ETV-027研究中HBeAg阴性的患者,第1、2年接受ETV 0.5 mg治疗,之后进入第2~5年的ETV-901后续研究,接受1.0 mg ETV治疗。LVD失效患者入组的是ETV-026研究中HBeAg阳性病毒学应答患者和部分无应答者,以及ETV-014及ETV-015研究中部分患者。
5年的耐药监测结果表明(图1),从第1年到第5年,核苷初治患者分别有663、278、149、120和108例接受了治疗和监测,第5年有93%患者的HBV DNA<300 copies/ml。在第5年没有患者出现ETV耐药突变T184、S202或M250以及LVD耐药突变M204I/V±L180M。5年ETV的累计基因型耐药发生率仅1.2%。
日本ETV临床Ⅱ期研究显示,核苷初治患者3年仅1例发生基因型耐药
日本大阪大学T. Takehara等进行的日本ETVⅡ期临床研究已经完成近3年的治疗。其中对核苷初治患者(ETV-047研究和ETV-053研究)分别治疗24或52周后,开放标签继续接受0.5 mg ETV治疗(ETV-060研究)。ETV-047研究中94%(32/34)的0.5 mg ETV治疗组患者和ETV-053研究中所有(34/34例)0.5 mg ETV治疗组患者进入了ETV-060研究,继续接受ETV 0.5 mg治疗。
数据显示,以ETV批准剂量(每日0.5 mg)连续治疗3年的58例初治患者中仅1例在148周发现ETV基因型耐药M204V、L180M和S202G。3年的累计基因型耐药发生率仅为1.7%(图2),通过对1例发生耐药的患者的基因测序分析发现,共产生了3个耐药位点突变(L180M+M204V+S202G)。
由此可见,日本ETVⅡ期临床研究的耐药数据与全球5年耐药监测数据吻合,再次证实ETV初治患者长期治疗的极低耐药发生率,并且ETV具有高耐药基因屏障,需要多个位点同时突变才能产生耐药。
恩替卡韦使患者以单药初始治疗并维持长期疗效,摆脱加药换药顾虑
众多指南均把HBV DNA的持续抑制作为CHB治疗的主要目标。作为指南的有力印证,R.E.V.E.A.L.-HBV研究结果不但证实了血清HBV DNA水平持续增高是发生HCC的强预测因子,并且揭示了低病毒血症仍有HCC风险,HBV DNA抑制得越低越好。
HBV DNA的持久强效抑制,不但需要核苷类药物具有强效抗病毒疗效,更加依赖于此类药物长期治疗的耐药发生状况,因为耐药的发生将抵消强效的抗病毒疗效,并给后续治疗的选择造成困难。ETV的全球临床耐药监测数据显示,在核苷初治患者中,ETV治疗5年累计基因型耐药发生率仅1.2%。日本ETV Ⅱ期研究再次从一个侧面证实了全球临床的耐药数据。ETV长期治疗保持极低耐药率是实现HBV DNA持久强效抑制的有力保障,使绝大多数核苷初治患者能够以1种单药开始治疗并且维持长期治疗疗效,摆脱加药或者换药的顾虑,从而实现慢乙肝长期治疗的策略。
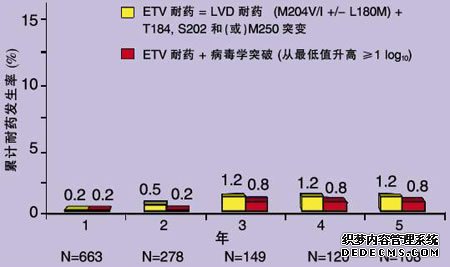 图1 核苷初治患者ETV治疗5年累计耐药发生率
图1 核苷初治患者ETV治疗5年累计耐药发生率
 图2 日本ETVⅡ期临床研究3年累计耐药发生率
图2 日本ETVⅡ期临床研究3年累计耐药发生率
责任编辑 张力
APASL 2008 会议特刊
下一篇:乙肝耐药专家共识解析